miR-28-5p-IL-34-žŪĘÉŧ°ûˇ´đģØ¡Õ{š¸Î°ŠŪDŌÆ
ÖÜŊĖĘÚŊŌĘž¸Î°ŠŪDŌÆĐÂCÖÆ
ÍĩŠ´ķWŖ¨¸ŊŲÖĐÉŊátÔēŖŠ¸Î°ŠŅĐžŋËųÖÜŊĖĘÚŅĐžŋFę ÔÚ2016Äę5ÔÂÕũĘŊ°ląíĄļHepatologyĄˇŖ¨¸ÎÅK˛ĄWŖŠësÖžĩÄÎÄÕÂ"miR-28-5p-IL-34-Macrophage Feedback Loop Modulates Hepatocellular Carcinoma Metastasis"Ŗ¨IF=11.19ŖŠĄŖŪDŌÆĘĮēĐÔÄ[Áö×îī@ÖøĩÄÉúÎīWĖØÕ÷ÖŽŌģŖŦŌ˛ĘĮÄ[ÁöģŧÕßËĀÍöĩÄÖ÷ŌĒÔŌōĄŖÄ[ÁöĩÄĮÖŌuŪDŌÆĘĮÄ[Áöŧ°ûĄĸËŪÖ÷ēÍÄ[ÁöÎĸhžŗÖŽégŌģĪĩÁĐÍësĩÄĐōØßBĀmß^ŗĖĄŖmicroRNAŖ¨miRNAŖŠŖŦͨŗŖēŦĶĐ22AģųĩÄļĖæˇĮž´aRNAŖŦͨß^ŪDäēķËŽÆŊÕ{ššĻÄÜģųŌōĩÄąíß_ŖŦ°l]Ą°°ŠģųŌōĄąģōĄ°ŌÖ°ŠģųŌōĄąĩÄšĻÄÜĄŖÖÜŊĖĘÚÕnî}ŊMͨß^ĘŠŌģĖ×ÍęÕûŋbÃÜĩÄŅĐžŋÁ÷ŗĖŖŦĻ
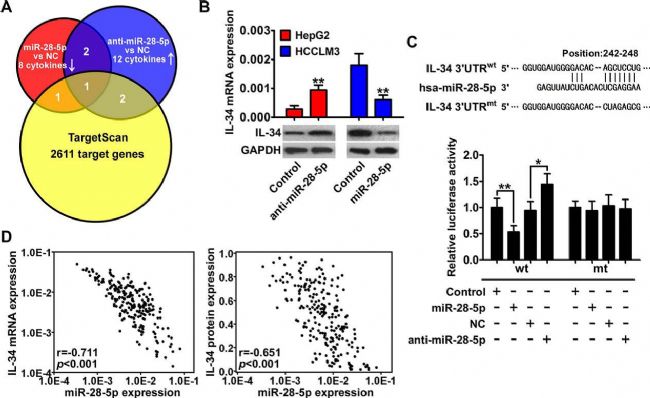
ĸÅc¸Î°ŠŪDŌÆĩÄęPæImiRNAsßMĐĐēYßx˛ĸĻÆäšĻÄÜÕšé_ĪĩÁĐŅĐžŋĄŖĘ×ĪČŖŦŅĐžŋČËTÔÚžßĶвģÍŦŪDŌÆÄÜĩÄČ˸ΰŠŧ°ûÖęßMĐĐRNA-seqēYßxŖŦ°lŦF¸Î°ŠŪDŌÆęPæImiRNAŖēmiR-28-5pąíß_ŽŗŖŖŦĮŌÅcŧ°ûĪĩŪDŌÆÄÜŗĘī@ÖøØĪāęPŖģÍŦr°lŦFmiR-28-5pÖģĘĮķwČžßĶĐ´ŲßM¸Î°ŠŪDŌÆĩÄ×÷ĶÃĄŖßMŌģ˛ŊŖŦß\ĶÃTargetScanÉúÎīĐÅĪĸWîAyŊYēĪŧ°ûŌō×Ķ/Ú
ģ¯Ōō×ĶPCRĐžÆŦßMĐĐēYßxō×CŖŦ°lŦFmiR-28-5pĩÄÖØŌĒ°ĐģųŌō°×ŊéËØ34 (Interleukin-34ŖŦIL-34)Ŗ¨ÕŌDŌģŖŠĄŖŧČÍųŅĐžŋąíÃ÷IL-34ÅcÎēËŧ°ûąíÃæąíß_ĩÄŧ¯Âä´Ėŧ¤Ōō×ĶĘÜķwCSFIRŊYēĪŖŦ´Ėŧ¤žŪĘÉŧ°ûģîģ¯ĄŖąž´ÎŅĐžŋ°lŦFŖŦIL-34ÔÚķwÍâŧ¤ģîFAKēÍERK1/2ĐÅĖͨ¡ŖŦ´ŲßMžŪĘÉŧ°ûÔöÖŗēÍÚ
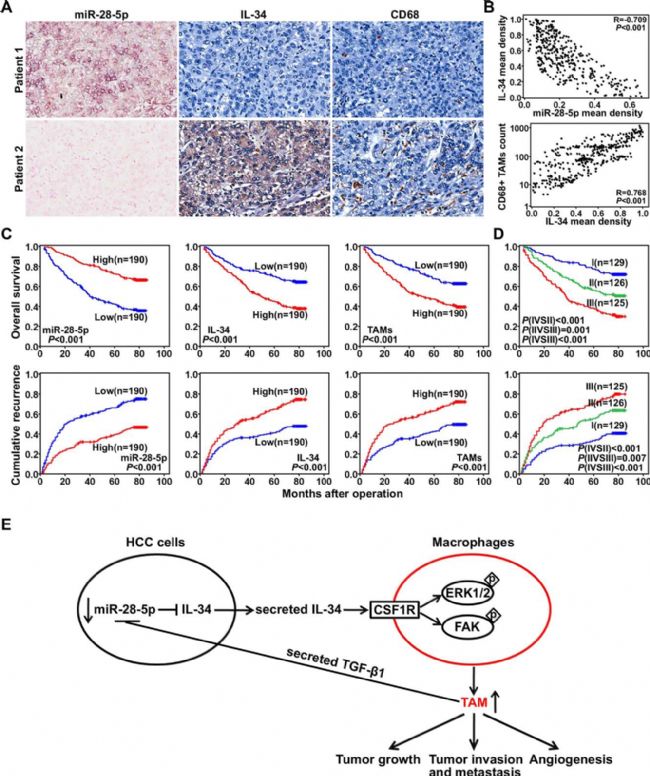
ģ¯ĄŖÔÚĶÎīōÖĐŖŦ¸Î°Šŧ°ûÖĐIL-34ĩÄÉĪÕ{´ŲßMÄ[Áöŧ°ûĩÄÉúéLŌÔŧ°ˇÎŪDŌÆŖŦÔöŧĶÁöČžŪĘÉŧ°ûŊūĄŖÖĩĩÃ×ĸŌâĩÄĘĮŖŦŅĐžŋÕß°lŦFžŪĘÉŧ°ûˇÖÃÚŧ°ûŌō×ĶTGF-ĻÂ1ĐÎŗɡ´đģØ¡
ĸÅcmiR-28-5pĻIL-34ĩÄÕ{ŋØžWŊjŖ¨ÕŌDļūŖŠĄŖ×îēķŖŦ¸Î°ŠĶąžÖĐÃâŌßŊMģ¯ˇÖÎöąíÃ÷ŖŦÁöŊMŋÖĐmiR-28-5p ÅcIL-34ąíß_ËŽÆŊī@ÖøØĪāęPŖŦÅcžŪĘÉŧ°ûĩÄŊūĄĸģŧÕßŋÉú´æÆÚļĖŌÔŧ°Ä[ÁöģŧÕßĩÄÍ°lī@ÖøĪāęPĄŖļā×ÁŋˇÖÎöī@ĘžŖŦmiR-28-5pĩÍąíß_/IL-34ß^ąíß_ģōÅcÁöČžŪĘÉŧ°ûÍŦr´æÔÚŖŦļŧĘĮŌģĒÁĸĩÄÕûķwÉú´æēÍ°Š°YÍ°lîAēķÖ¸ËŖ¨ÕŌDļūŖŠĄŖÔŅĐžŋŗÉšûÔėĐÔĩØĀLÖÆŗö¸Î°Šŧ°ûÖĐmicroRNAÅcÄ[ÁöĪāęPžŪĘÉŧ°û(TAM)ëpĪōÕ{ŋØžWŊjŖŦŊŌĘžÁ˸ΰŠŪDŌÆÕ{ŋØĐÂCÖÆēÍÔÚĩġÖ×Ķ°ĐücĄŖ
DŌģ°×ŊéËØ34 (Interleukin-34ŖŦIL-34)ĘĮ miR-28-5pĩÄÖØŌĒ°ĐģųŌōĄŖō˛ÉĶÃÉĪēŖŧĒPšĢËžĖᚊĩIJĄļžŨdķwĄŖ
DļūmiR-28-5pÅcÄ[ÁöĪāęPžŪĘÉŧ°û(TAM)ëpĪōÕ{ŋØžWŊjĄŖ
×÷ÕßēŊéŖēÖÜÉŲí˛ŠĘŋŖŦÍĩŠ´ķW¸ŊŲÖĐÉŊátÔē¸ÎÄ[ÁöÍâŋÆץÔēátŖŦÖ÷ŌĒÄʸΰŠŅ×°YÎĸhžŗÕ{ŋØÄ[ÁöĮÖŌuŪDŌÆĩÄCÖÆŅĐžŋŖŦŊüÎåÄęŌÔĩÚŌģ×÷ÕßÔÚGastroenterology ĄĸHepatologyĩČësÖžÕũĘŊ°ląíSCIÕÖø10ÆĒŖŦĀÛˇeĶ°íŌō×Ķ79.8ŖŦËûŌũ200Ķā´ÎĄŖÄŋĮ°×÷éÕnî}ØØČËÖ÷ŗÖøŧŌ×ÔČģŋÆWģųŊđĮāÄęģųŊđēÍÉĪēŖĘĐPˇĢĶÕnî}¸÷1íĄŖ
ÔÎÄŪD×ÔŖēŧĒPģųŌōÎĸĐÅšĢąĖ

éL°´ŧĶęP×ĸ
- ŌíēÍÉúÎīSNPģųŌōˇÖĐÍŧŧĐgŖēŊŌÃØģųŌōÃÜ´aŖŦĖŊ¤ŊĄŋĩ֎¡
- ´ŲÄIÉĪĪŲƤŲ|ŧ¤ËØáˇÅŧ¤ËØŖ¨CRHŖŠÔÚĖŊË÷ˇĘÅÖCÖÆÖĐĩÄŅĐžŋ
- ÃÚÄōĪĩŊyŧ˛˛ĄĩÄęPæIÖί°ĐücÖŽV2RĩÄŊéŊBŧ°ĪāęPō
- ŧ¤šâš˛žÛŊšī@ÎĸįRÖúÁĻÄ[ÁöŌÖÖÆŠŅĐžŋ
- ŋÕégļāŊMWŊâ´aÄ[ÁöÎĸhžŗŖŦÖúÁĻŧĶËŲžĢĘÖίŅĐžŋ
- ĀûĶÃÎŧ°ûŪDäŊMŧŧĐgŊâÎöļāˇNÃâŌßŧ°ûĻ´ķÁŋŧ°ûŌō×ĶĩÄíĒ
- EmulateÆ÷šŲĐžÆŦÖúÁĻŅĐžŋËÎīŌũÆđ¸ÎpûĩÄCÖÆ
- šĮŲ|ĘčËÉēÍŧ× îÅÔĪŲšĻÄÜpÍËęPæI°ĐücPTH1RĩÄŊYšĻÄÜŧ°ĪāęPōŊéŊB
- ÉúÎīĐžÆŦÍÆŗö"ĐžŋÕŌģĖ"ˇŊ°¸ÖØËÜŋÕégļāŊMWĐ¡ļĘŊ
- IPHASEÕnĖÃé_ÕnĀ˛ŖēŧžúģØÍÍģ×ÔōŗŖŌî}ÅcŊâ´đ
- ÉúÎīĐžÆŦÅcĐžŗŦÉúÎīÂēĪÍÆŗö"ĐžŋÕŌģĖ"ļāŊMWˇŊ°¸
- ÉúÎīátËzyÅcÔŠšŠĒÉĖŌíēÍÉúÎīĪōČĢøÕĐÄŧŊäNÉĖ
- žÉĪÕnŗĖŖēØiÄcĩĀšÚ ļžÅcČËķwoÂĩÄ´úÖxļˇ
- Ōģ×÷Öą˛ĨŖēŋšĐÔĩíˇÛͨß^ÖØËÜÄcĩĀÎĸÉúÎīČēžŊâˇĘÅÖ
- SBC&ÄŖģųÉúÎī2024ÄęĩÚŌģÆÚîÆ÷šŲŗõŧÅāĶ°āŅûÕē¯
- SBCŅûÄú ĸŧĶ2024ŋÕégļāžSŊMWĐÂŪDģ¯ŅĐĶū
Copyright(C) 1998-2025 ÉúÎīÆ÷˛ÄžW ëÔŖē021-64166852;13621656896 E-mailŖēinfo@bio-equip.com