安慰劑發揮鎮痛作用的神經環路機制詳解
2024年7月24日北卡羅來納大學教堂山分校Grégory Scherrer團隊在Nature雜志上以Accelerated Article Preview形式發表文章揭示了rACC→PN(腦橋核)環路參與安慰劑引起的鎮痛作用。

01、APC可產生期望依賴的鎮痛作用
研究人員建立安慰劑鎮痛條件性訓練實驗(APC)模擬安慰劑鎮痛效應,在適應期小鼠可自由穿梭在兩個底部30℃(非傷害性刺激)的箱子,經過三天適應后進行訓練期,1號箱子底部區域48℃(傷害性刺激),2號箱子底部區域30℃,經過三天訓練后小鼠停留在2號箱子區域時間增多,在測試期1和2號箱子底部區域均為48℃,檢測小鼠在1號和2號箱中的停留時間,結果發現小鼠在2號箱停留時間顯著增多。此外,經過APC訓練后小鼠在接受傷害性刺激(48℃)后首次出現舔舐前爪、首次直立、首次跳躍的潛伏時間均比未接受訓練的小鼠延長,表明APC可產生期望依賴的鎮痛作用。
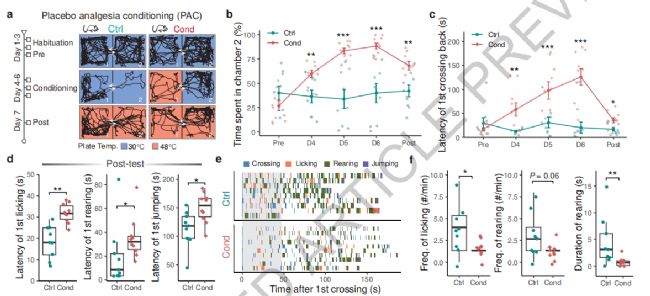
圖1、APC可產生期望依賴的鎮痛作用
02、rACC→PN環路參與APC引起的鎮痛作用
通過Fos-CreERT2工具小鼠發現APC訓練后吻側前扣帶皮層(rACC)神經元活性顯著增加,病毒示蹤工具rACC激活的神經元主要投射到紋狀體、未定帶區、腦橋核(PN)、背內側丘腦,其中PN接受的輸入最多。利用光纖鈣成像記錄系統發現rACC→PN環路神經元鈣離子活性在訓練期間逐漸升高,在測試期間鈣離子活性也顯著升高。電生理實驗發現APC訓練后rACC→PN神經元放電頻率增加,自發性興奮性突觸后電流增強,誘發的長時程增強作用更強,前饋抑制作用減弱。
測試期間光抑制rACC→PN環路可阻斷APC產生的鎮痛作用。在熱板實驗中光抑制rACC→PN環路縮爪潛伏期減少,激活該環路后小鼠縮爪潛伏期延長。在機械性刺激中光抑制上述環路縮爪頻率增加,激活該環路縮爪頻率減少,表明rACC→PN環路參與APC引起的鎮痛作用。
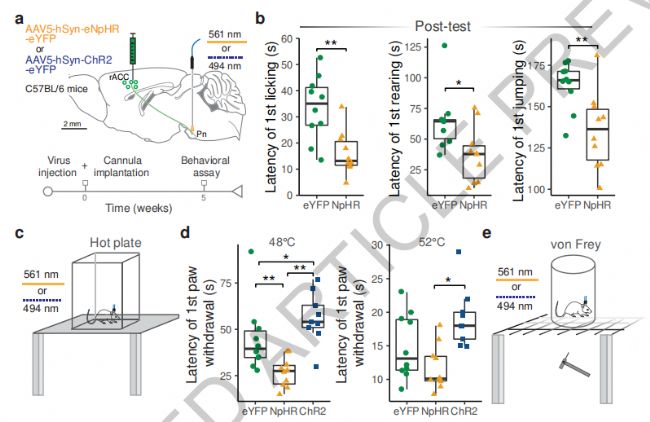
圖2、rACC→PN環路參與APC引起的鎮痛作用
03、Pn腦區神經元表達阿片肽類受體
單細胞測序實驗發現Pn腦區約72%神經元為興奮性神經元,約一半的神經元表達Oprd1 (編碼δ-阿片類受體),僅26%神經元表達Oprm1 (編碼μ-阿片類受體)。病毒示蹤實驗發現rACC投射到Pn-Oprd1神經元,光抑制Pn-Oprd1神經元可取消APC引起的鎮痛作用。藥理學實驗也發現δ-阿片類受體和μ-阿片類受體激動劑均能阻斷APC引起的鎮痛作用。此外,光抑制Pn-Oprd1神經元可增加小鼠機械性和熱覺敏感性。
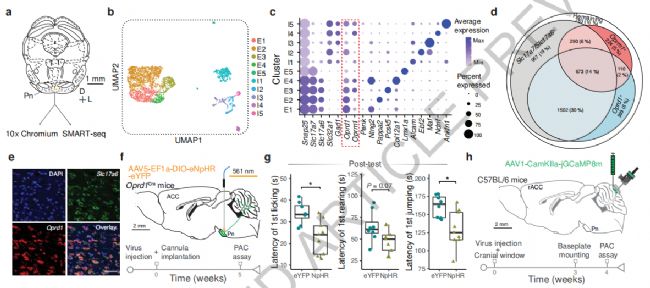
圖3、Pn腦區神經元表達阿片肽類受體
04、總結
本文通過建立APC模型模擬安慰劑鎮痛作用,基于該模型發現激活的rACC腦區神經元主要投射到Pn區域,抑制該環路可阻斷安慰劑相關的鎮痛作用。


想了解更多內容,獲取相關咨詢請聯系
電話:+86-0731-84428665
伍經理:+86-180 7516 6076
徐經理:+86-138 1744 2250