ÄÍļßû}šËËáÃļĩÄĖØücž°ÔÚÉúÎïátËîIÓōÖÐĩÄŠÓÃ
ÔÚÉúÎïátËÐÐIÖÐĢŽËÞÖũšËËáÁô§íĩÄïLëUēŧŋÉšöŌĄĢËÞÖũĩÄšËËáÁôĢŽĖØeĘĮ DNA ÁôþŌýČëÃâŌßÔÐÔĄĒÖÂÁöÐÔĄĒļÐČūÐÔĄĒļÉ_īúÖxĩČÔÚĩÄ°ēČŦïLëUĄĢļũøËÆ·ąOķ―đÜĀíCĶÉúÎïÖÆÆ·ĩÄËÞÖũšËËáÁôÁŋķžÓÐÖøĀļņĩÄÏÞķČŋØÖÆĄĢĀýČįĢŽĄķÖÐøËĩ䥷ĢĻ2020 °æĢĐŌķĻĢŽŌßÃįîËÞÖũDNAÁôŌŧ°ãŋØÖÆŠÔÚ0.05 - 10ng / ĐĢŧÃĀø FDA îCēžĩÄ·ĻŌÖÐŌŠĮóËÞÖũ DNA ÁôÐčŋØÖÆÔÚĩÍÓÚ10ng / ĐĢŽēĒĮŌDNAīóÐĄÐčÐĄÓÚ200bpĄĢ
ũ―yĩÄČŦÄÜšËËáÃļÔÚÖÐĄĒļßû}lžþÏÂŧîÐÔþžąĄÏÂ―ĩĢŽķøÉúÎïátËĩÄÉúŪaß^ģĖÖÐĢŽČįÔÚ AAV ĩČēĄķūÝdówĩÄÖÆäÖÐĢŽļßû}hūģŋÉŌÔÓÐЧpÉŲēĄķūîwÁĢĩÄūÛžŊĢŽĖáļßÆäĩÃÂĘĢŽÍŽrŌŧÐĐžŧŊđĪËŌēÐčŌŠÔÚļßû}lžþÏÂßMÐÐĄĢß@ūÍĘđĩÃũ―yšËËáÃļÔÚß@ÐĐĮérÏÂo·ĻMŨãČĨģýËÞÖũšËËáĩÄÐčĮóĢŽÔöžÓÁËÉúŪaģÉąūšÍđĪËÍësķČĄĢ
ÄÍļßû}šËËáÃļĩÄģöŽFt―âQÁËß@Ōŧëyî}ĄĢËüŋÉŌÔÔÚ·šĩÄû}âķČlžþÏÂąĢģÖļßЧÐÔĢŽÄÜōÓÐЧČĨģýËÞÖũšËËáĢŽ―ĩĩÍđĪËëyķČĢŽĖáÉýÉúŪaЧÂĘĄĢÄÍļßû}šËËáÃļÔÚÉúÎïátËÐÐIÖаl]ÖøÖÁęPÖØŌŠĩÄŨũÓÃĢŽéÉúÎïÖÆÆ·ĩÄ°ēČŦÐÔšÍÓÐЧÐÔĖáđĐÁËÓÐÁĶąĢÕÏĄĢ
Part1 ÄÍļßû}šËËáÃļĩÄŠÓÃîIÓō
ĢĻŌŧĢĐŌßÃįšÍēĄķūÓÆ·ÖÆä
ÔÚŌßÃįšÍēĄķūÓÆ·ÖÆäß^ģĖÖÐĢŽÄÍļßû}šËËáÃļ°l]ÖøÖØŌŠŨũÓÃĄĢÓÉÓÚÔÚÄģÐĐđĪËhđÖÐĢŽļßû}hūģŋÉŌÔŌÖÖÆēĄķūÝdówūÛžŊĄĒĖáÉýŪaÁŋĢŽŌōīËģĢģĢÐčŌŠÔÚļßû}lžþÏÂßMÐÐēŲŨũĄĢķøũ―yĩÄšËËáÃļÔÚļßû}hūģÏÂŧîÐÔþžąĄÏÂ―ĩĢŽo·ĻÓÐЧČĨģý DNA ÎÛČūĄĢÄÍļßû}šËËáÃļtÄÜōÔÚļßû}hūģÏÂąĢģÖļßŧîÐÔĢŽÓÐЧČĨģýŌßÃįšÍēĄķūÓÆ·ÖÐĩÄ DNA ÎÛČūĄĢ
ĢĻķþĢĐĩ°°ŨžŧŊ
ÔÚĩ°°ŨžŧŊ·―ÃæĢŽÄÍļßû}šËËáÃļŌēÓÐÖøV·šĩÄŠÓÃĄĢÅcž°ûŧōžūúÁŅ―âŌšÅäšÏĘđÓÃrĢŽÄÍļßû}šËËáÃļŋÉŌÔČĨģýīÖĖáÎïÖÐĩÄšËËáĢŽ―ĩĩÍČÜŌšÕģÐÔĢŽÄķøĖáļßĩ°°ŨŲ|ŪaÁŋĄĢīËÍâĢŽËüßÄÜÓÐЧČĨģý§ØëšÉĩÄšËËáĶëpÏō SDS-PAGE ĩ°°ŨÓÆ·ĩÄÓ°íĢŽļÄÉÆĩ°°ŨŲ|ĩÄ·ÖëxЧđûĢŽÔöķþūSëÓū·ÖąæÂĘĄĢĀýČįĢŽČŦÄÜšËËáÃļÔÚÖØ―Mĩ°°ŨžŧŊŧō―Mŋž°ûÓÆ·ĩ°°ŨĖáČĄrĢŽŋÉŌÔČĨģýšËËáÎÛČūĢŽÓÐЧ―ĩĩÍÓÆ·ÕģķČĢŽąãÓÚÏÂÓÎēŲŨũĄĢ
ĢĻČýĢĐÆäËûîIÓō
ÄÍļßû}šËËáÃļÔÚÆäËûîIÓōŌēÓÐÖøÖØŌŠĩÄÓÃÍūĄĢĀýČįĢŽËüŋÉŌÔpÉŲīæ·ÅĩÄÍâÖÜŅŠÎž°ûĢĻPBMCĢĐĩÄ―YKŽFÏóĄĢÔÚēŧŋÉČÜÐÔĩ°°ŨÍÐÔĮ°ļßŲ|Áŋ°üšówÖÆäß^ģĖÖÐĢŽÄÍļßû}šËËáÃļŋÉŌÔ―ĩ―âšËËáĢŽÓÐĀûÓÚ°üšówĩÄÖÆäĄĢīËÍâĢŽÔÚmNGSÖÐÓÆ·ĖĀíĩČß^ģĖÖÐĢŽÄÍļßû}šËËáÃļŌēÄÜ°l]ČĨģýšËËáĄĒļÄÉÆđĪËÁũģĖĩÄŨũÓÃĄĢĀýČįĢŽHL-SAN ÄÍļßû}šËËáÃļÔÚēĄÔÎĒÉúÎïÔ\āŠÓÃÖÐĢŽČįšęŧųŌō―MyÐōĢĻmNGSĢĐÓÆ·ČĨģýËÞÖũ DNA ·―ÃæąíŽFģöÉŦĄĢÍŽrĢŽÔÚĩ°°ŨžŧŊĢŽĖØeĘĮDNA―YšÏĩ°°ŨĩÄžŧŊß^ģĖÖÐĢŽŌÔž°ÆäËûÐčŌŠČĨģýËÞÖũDNAĩÄŠÓÃÖÐĢŽÄÍļßû}šËËáÃļķžūßÓЊĖØĩÄÝĄĢ
Part2 ÖðĩäÄÍļßû}šËËáÃļŪaÆ·ĖØüc
- ļßÃļŧîÐÔĢšÖÐĄĒļßû}ū_ŌšlžþÏÂĢŽÃļŧîÐÔļß
- ļßŧØĘÕÂĘĢšļßû}hūģÏÂpÉŲšËËáĀpĀ@ēĄķūŧōÄŋĩÄĩ°°ŨĢŽ―ĩĩÍAAVĩČēĄķūîwÁĢūÛžŊĢŽĖáļßÄŋĩÄŪaÎïŧØĘÕÂĘ
- ļßđĪËšąãÐÔĢšÏÂÓÎĘÕŦ@ŧōžŧŊoÐčģŽVQŌšŧōÍļÎöÃû}
Part3 ÖðĩäÄÍļßû}šËËáÃļÐÔÄÜōŨCĩþ
- PannaraseÄÍļßû}ČŦÄÜšËËáÃļ
PannaraseÔÚ150 mM Na+âķČlžþÏÂÃļŧîÐÔŨîļßĢŽ300 mMrČÔÓÐ36.2%ĩÄŧîÐÔ
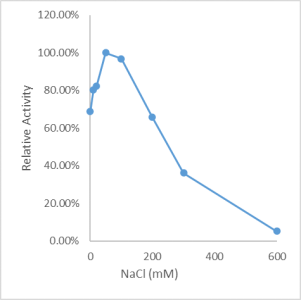
D1.PannaraseÄÍļßû}ČŦÄÜšËËáÃļÄÍû}Įúū
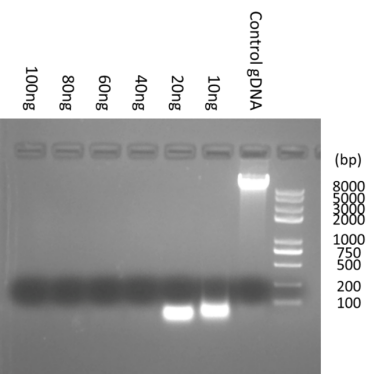
D2.PannaraseÄÍļßû}ČŦÄÜšËËáÃļÃļĮÐĩþ
PannaraseÄÍļßû}ČŦÄÜšËËáÃļĢĻSANĢĐĢŽļüļßû}ÄÍĘÜÐÍÔÚ600~700 mM Na+âķČlžþÏÂÃļŧîÐÔŨîļß
D3.PannaraseÄÍļßû}ČŦÄÜšËËáÃļĢĻSANĢĐĢŽļüļßû}ÄÍĘÜÐÍÄÍû}Įúū
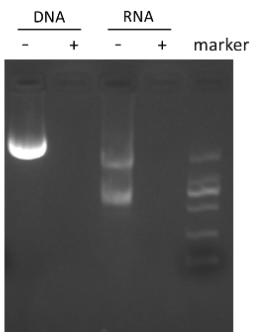
D4.PannaraseÄÍļßû}ČŦÄÜšËËáÃļĢĻSANĢĐĢŽļüļßû}ÄÍĘÜÐÍÃļĮÐĩþ
- PCL-PVAc-PEGÔÚŧîÐÔÎïßfËÍšÍÉúÎïēÄÁÏÉÏĩÄŠÓÃÝ
- PROTACßB―ÓŨÓÖÐŨũÓÃCÖÆž°ĩŠëshĩÄ―YÝÅcđĶÄÜĖØÐÔ
- OK432ÔÚÄ[ÁöšÍÃâŌßŅÐūŋÖÐĩÄŨũÓÃCÖÆž°ŠÓÃÝ
- čFÕ{ËØHepcidin-25ŨũéčFīúÖxšÍÃâŌß·īŠęPæIÕ{đŌōŨÓĩÄđĶÄÜšÍŨũÓÃ
- ĖĮĩ°°ŨFibronectinÔÚž°ûÅāðBÖÐĩÄđĶÄÜž°ŨũÓÃ
- TDP-43ĩÄ―YÅcđĶÄÜž°ÔÚuö°Y(ALS)ĩČÉņ―ÍËÐÐÐÔžēēĄÖÐĩÄŨũÓÃCÖÆ
- DNP-BSA(2,4-ķþÏõŧųą―ÅžÂÅĢŅŠĮå°Ũĩ°°Ũ)ÔÚÃâŌßWŅÐūŋÅczyÖÐĩÄŨũÓÃ
- AbMole LPSĢĻÖŽķāĖĮĢĐÔÚÃâŌßžĪŧîĄĒÓÎïÔėÄĢĩČ·―ÃæĩÄŠÓÞ°°ļĀý·ÖÏí
- MCEÖÐøĒyÔĐŪaÆ·ÁÁÏāÃĀøÖĨžÓļį2025 AACRÄęþ
- 2024Äę"MCEÖÐøÉúÃüŋÆWŅÐūŋīŲßMŠ"ÔuŠ―YđûđŦēž
- ĖÕÐgÉúÎïÖąēĨîAļæĢšĘÜówËĀíWÅcËÎï°lŽFŅÐūŋ
- °ē―ÝÃâŌß―MŧŊ·ĻPD-L1zyÔĐšÐŦ@ĩÃWÃËIVDRÕJŨC
- ĩÂøMassive PhotonicsÍÆģöķāŋîDNA-PAINTļũÏĩÔĐšÐ
- ĖėÂĄŨÔÖũŅаlHCVšËËázyÔĐšÐŦ@ÅúËąOūÖČýîNMPA
- ĖmēĐĀûĩÂÍÆģöÐÂÆ·ļßąĢÕæŋėËŲUÔö PCR mixÔĐšÐ
- IPHASEŅûÄúđēļ°BIOCHINA2025ĩÚĘŪÃŌŨŲQÉúÎïŪaIīóþ