D-螢光素鉀鹽作用原理及常見問題答疑
D-螢光素 (D-Luciferin) 是熒光素酶的常用底物。D-螢光素利用熒光素酶報告基因在活體內表達產生的熒光蛋白發生化學反應產生熒光,從而使用高靈敏度的光學檢測儀器檢測動物活體體內的細胞活動和基因行為,普遍應用于生物領域,特別是生物活體成像技術。
常見問題答疑
Q1.D-螢光素(D-luciferin)適合用于哪些實驗?
作為螢火蟲螢光素酶(Firefly luciferase)的作用底物,常常用于以下實驗:
1) 體內活體成像In vivo imaging;熒光素酶標記的腫瘤細胞、干細胞或傳染疾病通常注射入研究動物模型比如大小鼠內進行研究,從而對動物模型進行實時和非侵略性的監測疾病進程和/或藥效。
2) 體外研究In vitro study,包括熒光素酶和ATP水平分析;報告基因分析;高通量測序和各種污染檢測。
Q2.D-螢光素(D-luciferin)的作用原理如何?
作用機制:
在ATP和螢光素酶的作用下,D-螢光素((底物〉被氧化發光。當熒光素過量時,產生的光量子數與熒光素酶的濃度呈正相關性(見下圖)。
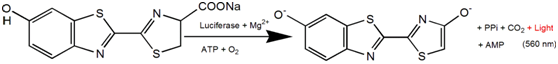
機理闡釋(體內)︰
熒光素酶(Luc)催化底物D-螢光素,利用ATP和Mg2+作為輔因子,氧氣存在下發射一典型的黃綠光,之后在體內37°C下遷移到紅光。
機理闡釋(體外)∶
很多因素都可能影響反應靈敏性,包括溫度、pH或底物濃度。建議使用pH 7.8的緩沖液,并且使用前將所有試劑預熱到室溫。建議反應緩沖液內添加過量的ATP和Mg2+以達到最佳反應狀態。
Q3.甲蟲熒光素(Beetle luciferin)和熒光蟲熒光素(Firefly luciferin)之間有差別?
兩者之間沒有差別,僅是不同公司命名上的差異,化學結構一致。
Q4.熒光素(luciferin)如何溶解,穩定性如何?
很多文獻和一些客戶提及用水溶解D-螢光素,之后置于-8OC分裝凍存,基本沒有明顯毒性效應。鉀鹽溶解性通常是60mg/ml,而鈉鹽溶解性高達100mg/ml(游離酸不溶于水,但溶于甲醇10mg/ml或DMSO50mg/ml)。
但是,關于溶解的D-螢光素穩定性存在爭議報道,可能由于水中含有的氧氣而破壞穩定性。最好將D-螢光素溶于無氣水 (degassed H20),保存效果最佳。對最靈敏的實驗,然而,強烈建議使用新鮮配制的反應液以降低實驗中的可變性(比如,低濃度酶或次優溫度或次優鹽離子濃度可能需要高濃度底物來驅動反應完全進行)。
Q5.D-螢光素鉀鹽和D-熒光素鈉鹽之間有差別?
兩者之間基本無差別,可能在物理特性上有些小差別,比如D-螢光素鈉鹽有點更顆粒狀和水溶性更由于鉀鹽。另外,從報道文獻來看約3倍多的文獻用鉀鹽,許多研究者體內更傾向于鉀鹽,但任何一種效果一致。
Q6.D-螢光素鉀鹽/鈉鹽和D-熒光素游離酸之問有差別?
D-螢光素游離酸不溶于水,除非溶于稀堿比如NaOH或KOH調整過pH的水。溶于甲醇10mg/ml或DMSO50mg/ml。然而,D-熒光素鉀鹽或鈉鹽在實驗中使用更方便,特別是體內成像,由于很容易溶于水或緩沖液,對檢測系統的毒性更低。
Q7.為什么D-螢光素鉀鹽/鈉鹽要溶于無Ca2+或Mg2+的PBS?其他鹽溶液能用于溶解D-螢光素鉀鹽/鈉鹽?
PBS,或磷酸緩沖鹽和DPBS都是生物學研究的常用緩沖鹽,通常用于細胞相關的研究中。PBS/DPBS是等滲緩緩沖液(比如與人身體兼容)。這些緩沖液專門設計能提供和維持穩定pH 7.2-7.6。PBS和DPBS之間沒差別,雖然后者無Ca2+/Mg2+。
鈣鎂溶液可能會限制胰酶活性。另外,Mg2+是催化D-熒光素生成氧化熒光素的關鍵成分(而Ca2+以相似的活性參與腔腸素催化)。其他鹽溶液可能用來溶解D-熒光素,只要存在的陽離子不會干擾實驗結果或產生脫靶效應。
Q8.D-螢光素在體內如何分布?
D-螢光素注射入動物體內后能快速分布且很容易分散到全身。
Q9.D-螢光素的體內發光動力性?
D-螢光素的給藥方式很多,常用的有腹腔注射、皮下注射和靜脈注射,不同的給藥方式動力學曲線有差異,見下圖片。對于大部分研究,腹腔/皮下注射約10-20min后達到熒光信號峰值,靜脈注射約2-5min達到信號峰值。
Q10.動物對重復注射D-螢光素的反應如何?
D-螢光素不會影響動物(沒有明顯毒性或免疫反應)。