空間代謝組學用于食管鱗狀細胞癌早期篩查的研究
代謝組學文獻分享—研究背景
近幾年代謝組學的研究如火如荼的開展,極大地促進了各學科的發展,如疾病診斷與治療、營養學、環境毒理學、進化和發育及藥物等;與此同時,質譜成像技術(mass spectrometry imaging, MSI)結合質譜分析和影像可視化,憑借其樣本處理簡單、能反應多種分子在空間上的分布及分子結構信息而受到高度的關注;尤其2004年Cooks等[1]將ESI源去掉封閉外殼,開發了常壓敞開式解析電噴霧離子化(DESI)技術并成功用于質譜成像分析,更促進了MSI在臨床醫學、藥學和植物學等領域的應用[2]。
代謝組學文獻分享,隨后,空間代謝組學(Spatial Metabolomics)也應運而生,它將組學信息擴展到了二維乃至三維的水平,研究小分子在組織切片中的空間分布,告訴我們變化“在哪里發生”,從而極大拓展了人們對組學樣品信息的認知[3-4]。

由于DESI等離子化技術需要被測樣品與采樣錐孔之間非常近,才能保證足夠高的靈敏度,而對于較大的組織樣品,無法將樣本放進離子化探針所在位置,難以將離子有效傳輸到質譜分析器進行高靈敏分析。
代謝組學文獻分享,鑒于此,藥物所“天然藥物活性物質與功能國家重點實驗室”再帕爾•阿不力孜教授課題組主導研發了新型敞開式空氣動力輔助離子化(Airflow-assisted desorption electrospray ionization,AFADESI)及其質譜成像技術(AFADESI-MSI)技術,借助0.5米或更長的傳輸管,實現了遠距離離子傳輸,放置樣品的空間非常充裕,且可輕松調整位置(圖1),并將該技術用于整體大鼠體內藥物成像分析[5-6]和腫瘤生物標志物的原位篩查及免標記分子病理診斷的研究[7-8]。
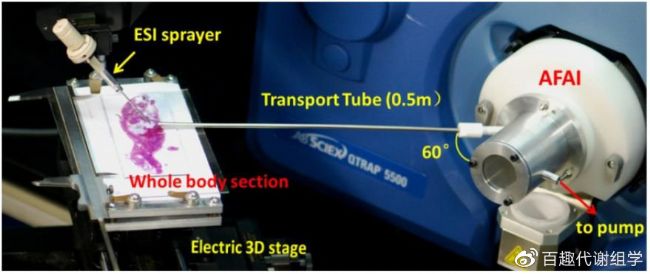
圖1 AFADESI-IMS系統[5]
近期,再帕爾·阿不力孜教授又將AFADESI-MSI技術與傳統免疫組織化學技術(Immunohistochemistry,IHC)進行結合,對256個患有食管鱗狀細胞癌(esophageal squamous cell carcinoma,ESCC)的病人的樣品進行組織空間特異性的代謝組學分析,實現了對腫瘤相關的代謝物和代謝酶進行高通量分析,并將其研究成果發表在PNAS上[9]。
本期文獻分享
Spatially resolved metabolomics to discover tumor-associated metabolic alterations. Proc. Natl. Acad. Sci. U.S.A. 2019 01 02;116(1)Proc. Natl. Acad. Sci. U.S.A. 2019 01 02;116(1). IF=9.580
代謝組學文獻分享—技術路線
為實現高通量原位檢測與腫瘤相關的代謝物和代謝酶,課題組首先利用AFADESI-MSI技術獲取不同組織(根據細胞類型和組成分為:癌癥組織、上皮組織和肌肉組織)空間特定區域的代謝物輪廓,再結合PLS-DA模型獲得ESCC和正常組織間的差異代謝物,隨后通過代謝通路分析選出可能與ESCC相關的酶;最后通過IHC技術用癌旁組織對與ESCC相關的酶進樣驗證(圖2)。
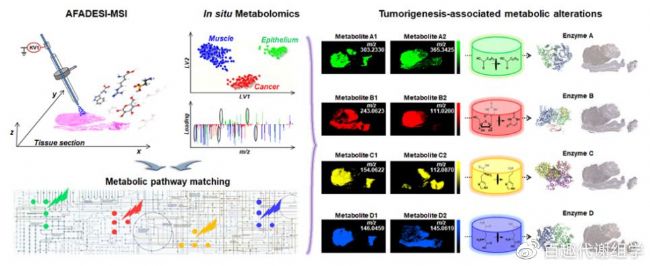
圖2 技術路線
代謝組學文獻分享—結果
通過該技術,能明顯發現甘油磷脂、葡萄糖酸、嘧啶、組氨酸、脂肪酸、精胺和脯氨酸在癌癥組織和正常組織中表達量的差異(圖3)。
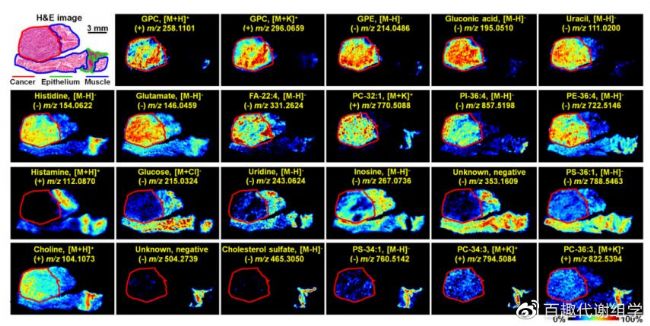
圖3 ESCC組織區域特異性空間分布圖
進一步的通路分析表明,脯氨酸合成、組氨酸代謝、谷氨酰胺代謝和脂肪酸合成等代謝通路在ESCC患者中發生改變,最后通過IHC驗證發現吡咯啉-5-羧酸還原酶2(PYCR2)、谷氨酰胺酶(GLS)、鳥苷磷酸化酶(UPase1)、組氨酸脫羧酶(HDC)、脂肪酸合成酶(FASN)和鳥氨酸脫羧酶(ODC)在癌癥組織中發生了紊亂,尤其是PYCR2和UPase1首次發現在ESCC中異常表達(圖4)。
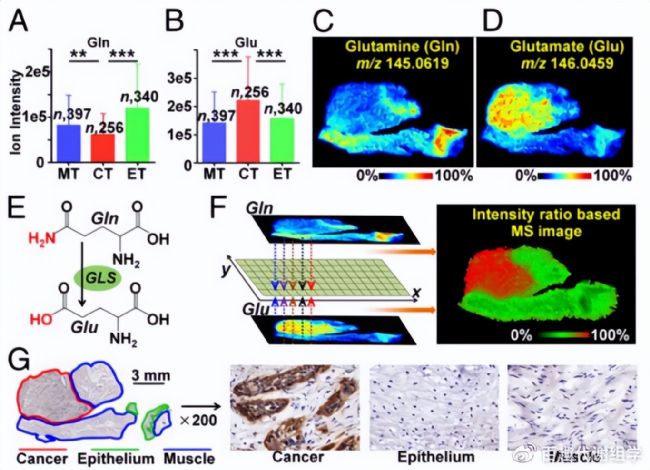
圖4 谷氨酰胺代謝通路中代謝物和酶的空間分布圖
代謝組學文獻分享,最后,課題組又用36個新收集的樣本進樣驗證,發現模型的準確率達到94.4%,且篩選的差異代謝物在不同組織樣本上的分布仍有較高的特異性。
結論
據報道[10],AFADESI-MSI的檢測靈敏度達到pg級水平,含量動態范圍跨越3個數量級,能檢測出1500多個代謝物,同時也能精確表征與識別代謝物在組織亞區域的分布特征;而本文將其與IHC方法結合,為研究癌癥的發病機制提供了代謝水平的分子依據,并為癌癥的診療干預提供了新的潛在靶點。
代謝組學文獻分享,隨著質譜成像技術、質譜成像可視化處理及定量等關鍵技術的不斷突破,以MSI技術為基礎的“空間代謝組學”也能為大家的研究提供新思路和新視角。