文獻解讀:代謝組學助力研究蛋氨酸飲食對人體癌癥與代謝情況的影響

百趣代謝組學文獻分享一篇題名 "Dietary methionine influences therapy in mouse cancer models and alters human metabolism",發表在Nature。文章是做的純代謝研究(飲食影響癌癥和代謝)。純代謝沖上Nature,這篇文章是怎么做到的呢?那接下來大家就跟隨小編一起來瞧瞧吧!

研究背景
我們經常會聽到人們說病從口入,這其實反映的是飲食對人體代謝的影響。在臨床上飲食干預通常用于輔助治療代謝病因方面的疾病,如生酮飲食、低脂飲食等。但飲食影響癌癥預后的原理還不是很明確。百趣代謝組學文獻分享,已經確定的是,利用藥物或輻射來靶向代謝途徑有時可以導致控制的治療結果。然而,飲食通過影響循環代謝物的水平來改變腫瘤的代謝途徑和影響治療結果的程度,還大部分是未知的。且目前還不清楚特定的飲食干預是否會影響標準癌癥治療中所針對的代謝途徑。對癌癥進行特定飲食干預的一種可能性是限制蛋氨酸(又稱甲硫氨酸)的攝入,蛋氨酸是一碳代謝中的一種必需氨基酸,且蛋氨酸是在人血漿中發現的最易變的代謝物,由于其在一碳代謝中的位置,決定它具有多種功能。
已有研究顯示,低蛋氨酸飲食可延長壽命并改善代謝健康。一碳代謝是5-氟尿嘧啶(5-FU)化療、放療等一線癌癥的靶點,在氧化還原和核苷酸代謝中發揮重要作用。
研究成果
蛋氨酸限制飲食迅速而特異性地改變了蛋氨酸和硫的代謝并抑制了腫瘤的生長
作者首先將C57BL/6J雄鼠隨機分為對照飲食組(0.86%蛋氨酸,w/w)和蛋氨酸限制飲食組(0.12%蛋氨酸,w/w),然后分不同時間點取小鼠血漿做代謝組學檢測(圖1a)。百趣代謝組學文獻分享,利用奇異值分解(圖1b)研究代謝動力學,并研究了蛋氨酸和硫代謝的協同變化(圖1b, c)。結果發現限制蛋氨酸攝入在兩天內降低了蛋氨酸相關代謝物的水平,并且這些水平在整個干預期間基本保持不變(圖1d)。
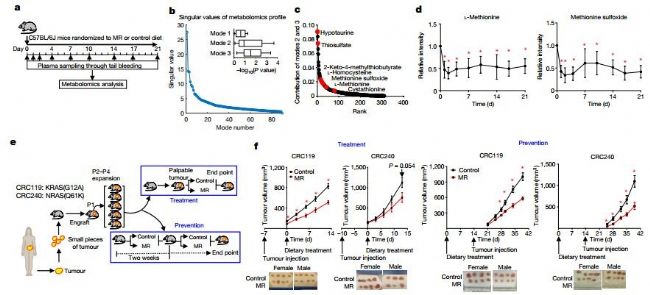
圖1
鑒于觀察到的這些快速而具體的影響,作者又在一系列與一碳代謝相關的臨床前設置中評估蛋氨酸限制的影響。百趣代謝組學文獻分享,作者使用了兩種RAS基因驅動的結直腸癌患者來源的異種移植(PDX)模型,其中一種(命名為CRC119)攜帶KRAS(G12A)突變,另一種(命名為CRC240)攜帶NRAS(Q61K)突變。
當腫瘤生長到一定大小時(治療環境設置)或在接種前兩周(預防環境設置),給予小鼠對照飲食或蛋氨酸限制飲食(圖1e)。發現蛋氨酸限制對CRC119腫瘤和CRC240腫瘤的生長都有抑制作用(圖1f)。為了深入了解代謝方面的變化情況,作者分析了腫瘤、血漿和肝臟的代謝物,發現在每種情況下,限制蛋氨酸都會改變蛋氨酸和硫相關的代謝(圖2c-e)。
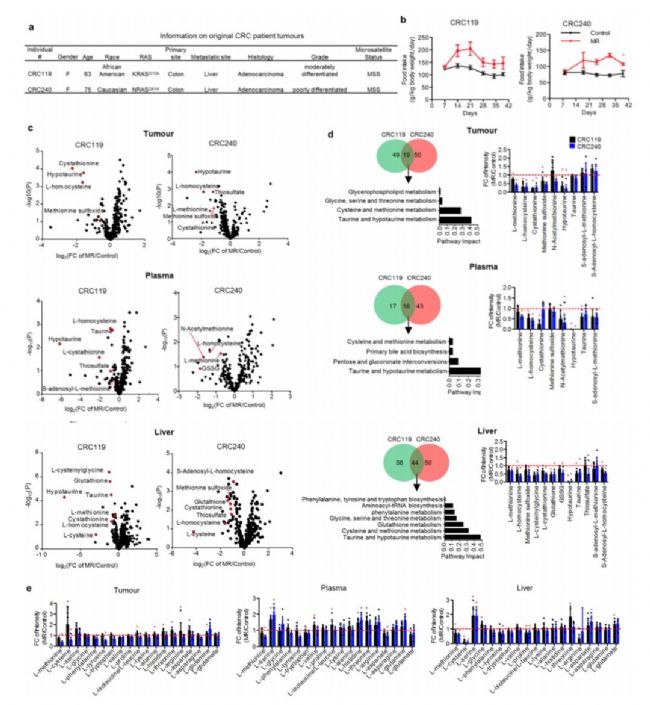
圖2
蛋氨酸限制使大腸癌的PDX模型對5-FU化療敏感
5-FU以胸苷酸合成酶為靶點,是治療結直腸癌的一線化療藥物,但其療效一般(約60-65%)。百趣代謝組學文獻分享,因此,作者在CRC119模型中測試了蛋氨酸限制是否能與5-FU協同作用(圖3a)。給予小鼠可耐受的低劑量5-FU,發現5-FU單獨作用對腫瘤生長沒有影響(圖3b)。蛋氨酸限制與5-FU協同治療,會明顯抑制腫瘤生長,最顯著的是,與5-FU和蛋氨酸限制的作用機制相關的核苷酸代謝和氧化還原狀態的變化(圖3b-d)。因此,蛋氨酸限制與5-FU協同作用,抑制結直腸癌腫瘤的生長,擾亂核苷酸代謝和氧化還原平衡。
接下來,作者在蛋氨酸限制、5-FU或兩者同時存在的情況下,向CRC119細胞和HCT116大腸癌細胞中補充了與蛋氨酸代謝相關的營養物質(圖3e)(藍色標記的為添加的代謝物)。百趣代謝組學文獻分享,發現核苷和N -乙酰半胱氨酸(NAC),以及相關的補充物,在CRC119細胞中,無論是否經過5-FU處理,都部分緩解了蛋氨酸限制引起的細胞增殖抑制(圖3f)。
使用帶有13C標記的絲氨酸(U-13C-serine)發現,限制蛋氨酸和5-FU導致5-FU引起的[M + 1] dTTP進一步降低,而增加[M + 1]蛋氨酸(圖3g, h)。因此,限制蛋氨酸和5- FU處理之間的協同效應至少部分是由于蛋氨酸合成的增加,它與dTMP合成的絲氨酸衍生的一個碳單元5,10-甲基四氫葉酸鹽競爭。由這些數據得出,破壞核苷酸代謝和氧化還原平衡有助于由蛋氨酸限制誘導的細胞增殖抑制。
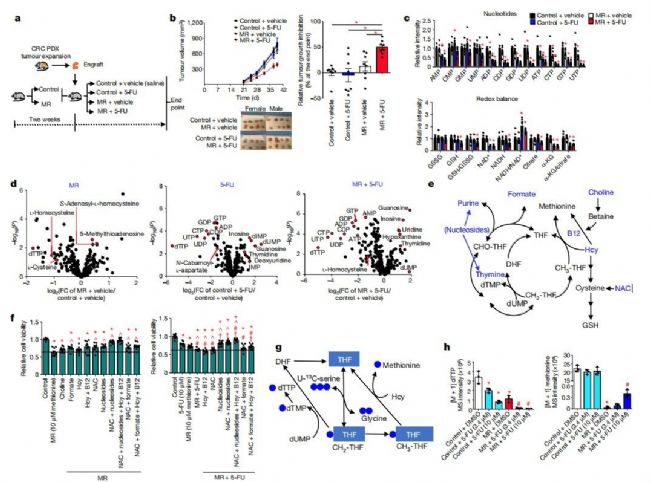
圖3
蛋氨酸限制使RAS驅動的自發性肉瘤小鼠模型對放射敏感
為了進一步探索飲食限制蛋氨酸的治療潛力和相關機制,作者采用了一種自體生長的軟組織肉瘤耐輻射小鼠模型。FSF-KrasG12D/+;Trp53FRT/FRT小鼠肌內注射表達FlpO重組酶的腺病毒后2 ~ 3個月內誘導肢體肉瘤(圖4a)。百趣代謝組學文獻分享,發現,蛋氨酸限制下的局部放射(20 Gy)可以減少腫瘤的生長,使腫瘤的生長時間延長三倍,從平均17.48天延長到26.57天(圖4c),這與已知的放療增敏劑的效果相當。且觀察到核苷酸和氧化還原相關代謝的破壞,這可能是蛋氨酸限制與放療聯合作用的結果(圖4d,e)。
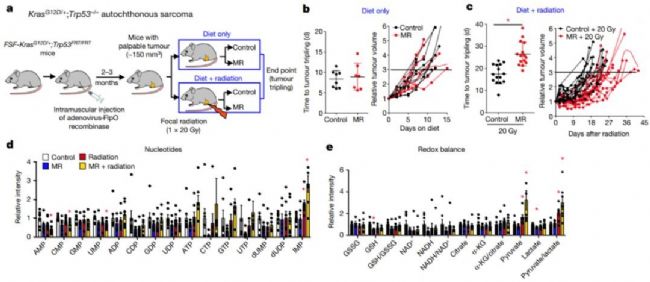
圖4
蛋氨酸限制在人體飲食中的研究
那么蛋氨酸限制飲食是否會同樣影響健康人體的代謝呢?
最后作者招募了6名健康的中年人,讓他們吃低蛋氨酸的食物(約2.92 mg/kg每天),相當于每日蛋氨酸攝入量減少83%,持續3周(圖5a)。研究發現,蛋氨酸限制可重復地抑制蛋氨酸水平和改變循環代謝,其中半胱氨酸和蛋氨酸代謝是改變最多的代謝途徑(圖5b)。百趣代謝組學文獻分享,蛋氨酸限制減少了所有受試者的N -乙酰半胱氨酸(NAC)和谷胱甘肽,并影響了與甲基化、核苷酸代謝、三羧酸循環和氨基酸代謝相關的代謝物(圖5b, c)。且健康人血漿蛋氨酸相關代謝物與所有小鼠模型的代謝物高度相關(圖5d),表明人與小鼠對蛋氨酸限制的反應是相似的。
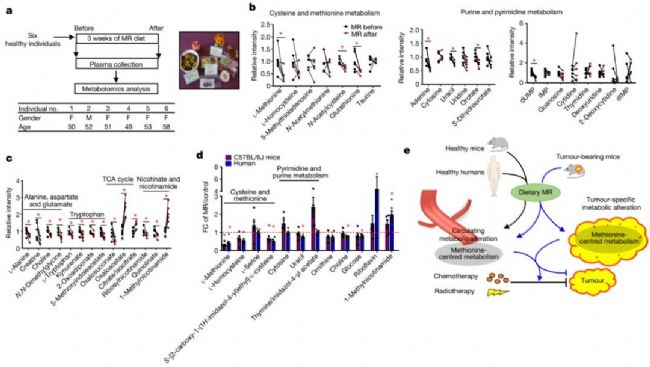
圖5
文章結論
總之,該研究表明,低蛋氨酸飲食可以在小鼠和人類中誘導快速和特異的代謝譜,而這種代謝譜可在臨床環境中被誘導。百趣代謝組學文獻分享,通過用蛋氨酸限制破壞一碳代謝的通量主鏈,會產生涉及氧化還原和核苷酸代謝的脆弱性,并且可以通過針對癌癥代謝這些方面的其他療法(本研究采用放療法和抗代謝藥物化療法)加以利用(圖5e)。
小趣結語:以上就是該文章的主要研究結果啦,所以大家看出來該研究就做了個代謝組就沖上了《Nature》的奧秘了嗎?
小趣覺得,首先,作者的研究思路是比較清晰的,且是環環相扣的關系。百趣代謝組學文獻分享,作者先通過低蛋氨酸飲食對小鼠的代謝影響靶向了低蛋氨酸影響的代謝物及代謝途徑;再緊接著研究了低蛋氨酸飲食對小鼠腫瘤模型代謝的影響及相關代謝物的變化情況;因為飲食療法通常會與臨床一線治療法相結合,所以作者也結合了臨床上對腫瘤的化療和放療方法,驗證低蛋氨酸飲食是否能起到協同作用的效果;最后結合了人體試驗,驗證低蛋氨酸飲食對人體代謝的影響是否與小鼠體內是一致的。
其次,應該是在數據分析上做的比較全面了,雖然沒有大量的樣本數,也沒有結合多組學,但作者將代謝組的數據得到了深入的挖掘,總結了低蛋氨酸飲食靶向的代謝物種類及代謝途徑,對應用于臨床具有切實的理論基礎。