伯豪客戶在自然通訊發表自身免疫性疾病重要研究成果
伯豪客戶在《自然通訊》(Nature Communications)雜志上接連發表自身免疫性疾病發病機制重要成果
研究意義
自身免疫性疾病與個體遺傳學特征,個人免疫系統,外界環境等有密切關系,有關自身免疫疾病的發病機制,特別是非編碼RNA在其中的調控角色還不是很清楚。來自上海交通大學醫學院的研究人員近期在《自然通訊》(Nature Communications)雜志上發表了兩篇有關miRNA在自身免疫性疾病中的調控作用研究成果,為更好的理解自身免疫性疾病的發病機制以及miRNA可能在自身免疫疾病中的治療前景提供了有力證據。
研究思路

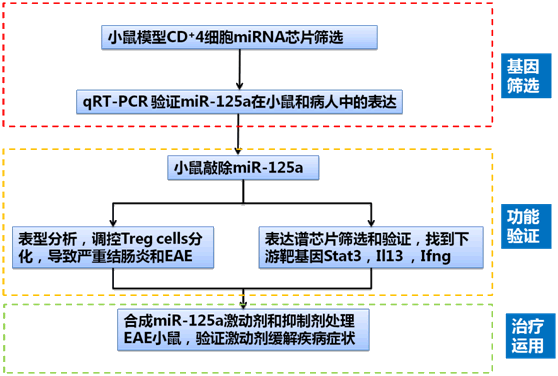
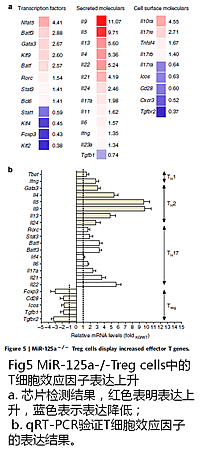 在第一篇文章中,研究人員首先通過芯片檢測了人紅斑狼瘡癥的MRL/lpr小鼠模型和多發硬化癥(EAE)小鼠模型脾臟CD4+ T細胞,發現miR-125a-5p顯著性下調。qRT-PCR驗證顯示,相比正常人,系統系紅斑狼瘡病病人和克羅恩病病人的 miR-125a表達下調。這些結果證明,miR-125a在小鼠模型和人的自身免疫性疾病中是特異性下調的。
在第一篇文章中,研究人員首先通過芯片檢測了人紅斑狼瘡癥的MRL/lpr小鼠模型和多發硬化癥(EAE)小鼠模型脾臟CD4+ T細胞,發現miR-125a-5p顯著性下調。qRT-PCR驗證顯示,相比正常人,系統系紅斑狼瘡病病人和克羅恩病病人的 miR-125a表達下調。這些結果證明,miR-125a在小鼠模型和人的自身免疫性疾病中是特異性下調的。為了進一步探究miR-125a功能,研究人員在小鼠模型中敲除了miR-125a。流式細胞分析發現,miR-125a的敲除影響了T細胞向調節性T細胞(Treg cells)的分化。而這種變化使小鼠從免疫抑制轉換為炎癥,導致了更嚴重的結腸炎和實驗性自身免疫性腦脊髓炎(experimental autoimmune encephalomyelitis,EAE)發病。
為理解miR-125a的分子功能,研究人員將miR-125a敲除小鼠和對照小鼠的CD4+CD25hi Treg細胞進行了表達譜芯片檢測。結果顯示輔助T細胞通路相關基因表達發生變化。結合miRNA靶基因預測,熒光素酶報告系統檢測和后期實驗結果,發現miR-125a可抑制T細胞效應因子Stat3,Il13 ,Ifng的表達。
研究人員通過人工合成不同劑量miR-125a,轉化CD4+ T細胞,發現內源的轉錄因子Stat3蛋白產生劑量依賴的表達抑制,Ifng 和Il13的mRNA表達也顯著性降低。
為了探究miR-125a的臨床治療前景,研究人員將合成的miRNA激動劑和抑制劑注射多發性硬化癥(EAE)小鼠,發現小鼠的癥狀在激動劑下顯著好轉,抑制劑下癥狀更加嚴重。
這些研究表明,在控制自身免疫性疾病過程中,miR-125a通過調控T細胞效應因子Stat3,Il13 ,Ifng的表達,影響了調節性T細胞的免疫穩態過程。這些結果為理解miRNA在自身免疫性疾病中的調控作用及miRNA用于免疫性疾病的治療作用提供了強有力的依據。該研究中Affymetrix GeneChip Mouse Genome 430 2.0芯片服務由上海伯豪生物技術有限公司提供。


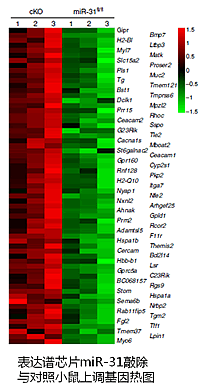 在第二篇文章中,研究人員首先檢測了多硬化癥小鼠模型(EAE)CD4+T細胞,發現miRNA-31表達比正常小鼠明顯升高。用TCR信號(plate-coated anti-CD3-和 soluble anti-CD28-特異性抗體)刺激初始T細胞,發現miR-31的表達顯著增加。在體外誘導Treg細胞(iTreg)細胞中,miR-31表達減少,TH1,TH17細胞中表達增加。ChIP實驗表明,FoxP3可能通過結合miR-31啟動子區進而影響了iTreg細胞中的miR-31表達。
在第二篇文章中,研究人員首先檢測了多硬化癥小鼠模型(EAE)CD4+T細胞,發現miRNA-31表達比正常小鼠明顯升高。用TCR信號(plate-coated anti-CD3-和 soluble anti-CD28-特異性抗體)刺激初始T細胞,發現miR-31的表達顯著增加。在體外誘導Treg細胞(iTreg)細胞中,miR-31表達減少,TH1,TH17細胞中表達增加。ChIP實驗表明,FoxP3可能通過結合miR-31啟動子區進而影響了iTreg細胞中的miR-31表達。為了進一步探究miR-31的功能,研究人員條件性地敲除了CD4+T細胞中的miR-31,然后誘導EAE,發現敲除小鼠的癥狀比對照組明顯減弱。進一步檢測發現,在發炎的脾臟和中樞神經系統中,敲除小鼠的TH1和TH17比例明顯減少,而外周Treg-cell(pTreg)的比例和總數卻明顯增加,表明miR-31影響了外周Treg-cell的穩態平衡。同時,通過分離初始T細胞后發現,敲除小鼠T細胞有更多的pTreg-cell產生,這對于EAE的發展起重要作用。
為了確認miR-31的具體功能機制,研究人員通過表達譜芯片和預測發現,敲除miR-31小鼠中的Gprc5a表達上升。熒光素酶報告系統證實,miR-31可靶定Gprc5a的3’UTR區進而調控其表達。
通過檢測誘導EAE和對照小鼠,研究人員發現Gprc5a的mRNA表達量和蛋白表達量明顯升高。在小鼠中敲除Gprc5a后,iTreg-cell明顯減少。把敲除小鼠進行EAE誘導,pTreg-cell的比例明顯少于對照,癥狀也比對照組嚴重。當把小鼠施與miR-31和Gprc5a雙敲除,EAE的癥狀嚴重程度恢復了miR-31單敲除時的減輕,表明在EAE發展過程中,miR-31通過調控Gprc5a來起作用。
這些研究結果表明,在自身免疫過程中,miR-31通過調控Gprc5a的表達,抑制了pTreg-cell的形成,通過調控miR-31及其靶基因可以對自身免疫反應進行定向調節。該研究中Mouse genome-wide cDNA microarray服務由上海伯豪生物技術有限公司提供。
研究亮點
這兩篇文獻都是對自身免疫性疾病發病機制中miRNA的作用進行了報道,兩篇文獻有相似的研究背景,相似的實驗設計,但是側重點不同,各有千秋。在第一篇研究中,除了研究miRNA在自身免疫性疾病中的作用,芯片尋找下游靶基因外,還用外源合成miRNA激動劑和抑制劑進行了靶向治療嘗試,可以說是機制和運用的完美結合。在第二篇研究中,有著類似第一篇一樣研究思路,但是在miRNA對靶基因的調控機制,以及他們之間如何具體影響自身免疫疾病發展等方面做了更加詳細的研究,可以說是一片非常優秀的信號通路研究文獻。
- 真邁FASTASeq 300 Dx獲批NMPA三類醫療器械注冊證
- 康寧公布2025年第一季度財務業績,強勁表現超出預期
- 慧榮和作為代表出席首屆專精特新小巨人企業生態大會
- 瑞孚迪與西湖維泰達成戰略合作共拓產前篩查新時代
- 碩果累累!谷豐光電與高校、科研機構合作成果盤點
- 復納亮相西交大分析測試論壇,深入剖析離子研磨技術
- 易科泰與法國 YellowScan 共探激光雷達市場新機遇
- 第十個中國航天日,回顧維拓啟創與中國航天的十年
- 10x Genomics技術方案更新(3月),新手冊邀您下載
- 易科泰受邀參加“十百千萬”農業新質人才培養工程
- 湘儀與重慶東暉簽約戰略合作伙伴
- Cytiva思拓凡:揚帆計劃-走入鼎康生物活動圓滿舉行
- 國儀量子EPR交流會福州大學站成功舉行
- 諾澤流體科技與德國Miccados GmbH正式達成戰略合作
- 蔡司ZEN core 軟件現可適配蔡司全系列掃描電鏡產品
- BSI邀您參加蛋白質組學數據分析培訓會
- 單細胞空間多組學技術論壇暨廣州站生信培訓班報名中
- SBC單細胞及空間多組學實驗與生信分析培訓班招生
- 小海龜發布百個橫向課題、千篇SCI-生命科學合作計劃
- 空間多組學研究策略及生信分析培訓班火熱招生中
- SBC ToolBox云平臺VIP專區再添新模塊GSEA數據分析
- SBC芯云講壇:國家自然科學基金的準備和申報技巧
- 第十期SBC單細胞及空間轉錄組測序培訓班報名通知
- 講座:器官芯片在藥物研發的應用及小分子藥物分享
- 第三屆單細胞空間多組學技術與應用研討會邀請函
- 4月盛會邀約場場精彩,伯豪生物誠邀您參會
- SBC專家講座:國自然標書撰寫策略及寫作技巧全攻略
- 伯豪生物2023春節放假與實驗室樣本接收事項通知
- 伯豪講座:單細胞和空間轉錄組技術解析腫瘤治療靶點
- 百趣生物直播:大咖坐鎮國自然線上講座,更有禮相送
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com






